Oksijen ve Karbondioksitin Taşınması
- 31 Tem 2025
- 2 dakikada okunur
Oksijenin vücutta etkili biçimde taşınmasını sağlayan ana unsur, damarlarımızda kesintisiz dolaşan kandır. Oksijen molekülünün suda çözünürlüğü oldukça düşüktür; bu nedenle kan plazmasında serbest halde taşınabilen O2 miktarı yalnızca %1,5 civarındadır. Kalan büyük oranda oksijen (%98,5), eritrositler içindeki hemoglobin moleküllerine bağlanarak taşınır ve dokulara ulaştırılır.
Bir hemoglobin molekülü, yapısındaki dört demir atomu sayesinde dört O2 molekülüne bağlanabilir. Hemoglobinin oksijenle olan bu bağlanması tamamen geri dönüşümlüdür; oksijenin bol olduğu ortamlarda hemoglobin kolaylıkla oksihemoglobin halini alırken, oksijen azaldığında ise tekrar deoksihemoglobin formuna döner. Bu özellik, oksijenin dokulara etkin şekilde ulaştırılmasını sağlar.
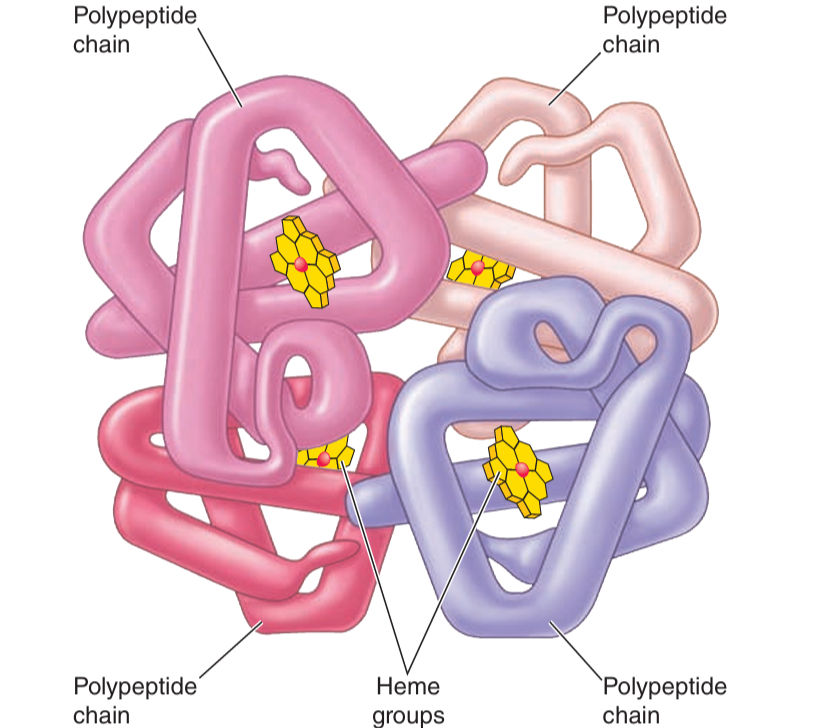
GÖRSEL Hemoglobin ve hem-demir yapıları
Kütle etkisi yasası gereği, ortamdaki oksijen yoğunluğu arttıkça hemoglobinin bağladığı O2 miktarı da artar; bu durum oksijenin taşınmasında temel bir dinamik oluşturur. Örneğin, sistemik arterlerdeki 100 mL kanda yaklaşık 20 mL oksijen bulunur ve bu denge, vücut ihtiyaçlarına göre hassas biçimde düzenlenir.
Dinlenim halinde bir kişiden alınan 100 mL sistemik venöz kan, ortalama 53 mL karbondioksit içerir. Bu CO2, kanda üç farklı biçimde taşınır: çözünmüş gaz halinde, karbaminohemoglobin olarak ve bikarbonat iyonu şeklinde. Her bir formun taşınma kapasitesi ve fizyolojik önemi farklıdır; bu çeşitlilik, CO2'nin verimli şekilde uzaklaştırılmasını sağlar.
Kan plazmasında çözünmüş halde bulunan CO2 oranı yaklaşık %7’dir. Akciğerlere ulaşan bu formdaki CO2, doğrudan alveol boşluğuna difüze olur ve solunum yoluyla atılır. Eritrositlerde hemoglobine bağlanarak taşınan CO2 oranı ise yaklaşık %23’tür; hemoglobin ve CO2'nin bu birleşimine karbaminohemoglobin adı verilir.

GÖRSEL Taşınma şekli ve oranlar
Karbaminohemoglobin oluşumu, pCO2 değerine duyarlıdır. Dokularda pCO2 yüksek olduğunda hemoglobine daha fazla CO2 bağlanır; pulmoner dolaşıma ulaşıldığında ise düşük pCO2 nedeniyle karbaminohemoglobin çözülür ve serbest kalan CO2 akciğerler yoluyla vücuttan atılır. Bu dinamik, gaz değişiminin temelini oluşturur.
Kandaki CO2’nin en büyük kısmı, yani yaklaşık %70’i bikarbonat iyonları şeklinde taşınır. CO2, eritrositlerde suyla birleşerek karbonik asit (H2CO3) oluşturur; karbonik anhidraz enzimi ise bu asidi hızla H+ ve HCO3- iyonlarına ayrıştırır. Bu kimyasal dönüşüm, CO2'nin taşınmasında kritik bir rol oynar.

GÖRSEL Dokularda gazların değişimi
Artan HCO3- konsantrasyonu, iyonların bir kısmının eritrosit dışına çıkmasına yol açar ve hücrede negatif yük kaybı meydana gelir. Bu yük dengesizliği, klorür iyonlarının eritrosit içine girmesiyle dengelenir; bu olaya "klorür kayması" (chloride shift) denir ve asit-baz dengesinin korunması açısından oldukça önemlidir.
Akciğerlerde, bu reaksiyonlar tersine döner; bikarbonat tekrar CO2’ye dönüştürülür ve gaz halinde solunum yoluyla vücuttan atılır. Deoksihemoglobin, oksihemoglobine göre yaklaşık 3-4 kat daha fazla CO2 taşıyabilir. Bu özellik, dokulardan CO2’nin uzaklaştırılmasında hemoglobinin etkinliğini artırır.
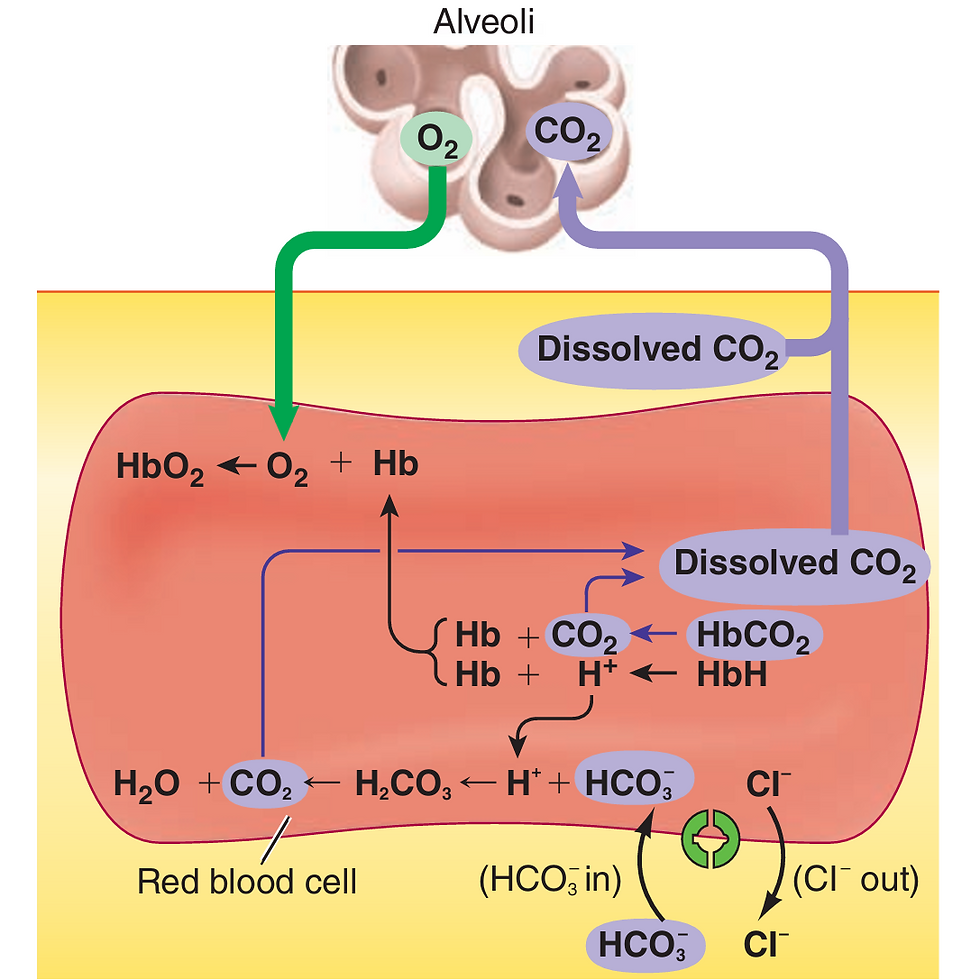
GÖRSEL Akciğerde gazların değişimi
Karbondioksit, hemoglobinin globin zincirindeki amin gruplarına bağlanırken; oksijen ise hem grubundaki demir atomuna bağlanır. Haldane etkisi, hemoglobinin oksijenle doyma derecesine göre CO2 bağlama kapasitesinin değişmesi anlamına gelir; bu, hem yapısal değişiklikler hem de amin gruplarının kullanılabilirliğiyle ilişkilidir.
Sonuç olarak,
Konuya ilişkin bilginizi tamamlamak ve kendinize seviye atlatmak için önceki ve sonraki yazılara göz atmayı ihmal etmeyin. Linklere aşağıdan ulaşabilirsiniz.
SSPS - level up yourself
Bu ve sitemizde yer alan diğer yazılar SSPS spor ve sağlık bilimleri kütüphanesi kaynakları kullanılarak hazırlanmıştır.



